Por: Prof. Roberto N. Onody *
Caro leitor,
O tema “Células-Tronco e a Medicina Regenerativa” pela sua extensão e complexidade foi dividido em 3 partes. Esta é a parte 3 ( veja parte 1 e parte 2). Devido às suas inúmeras aplicações no tratamento e, em alguns casos, até da cura de doenças graves, a importância das células tronco cresce dia a dia. Juntos, o transplante de células tronco e a terapia genética, representam hoje a vanguarda da medicina regenerativa.
Aproveito para informar que a newsletter “Ciência em Panorama” no. 4 já está no ar. Abaixo, um sumário da edição
*Astronomia
1-Um buraco negro supermassivo semeando novas estrelas?
2-Um buraco negro solitário
*Biologia
Qual é a árvore mais velha do mundo?
*Inteligência Artificial
Prêmio recusado
*Curiosidades Editoriais
*Curiosidades Matemáticas
A newsletter pode ser subscrita por qualquer pessoa, alunos, docentes, funcionários etc. Para receber as edições basta enviar um e-mail para
colocando o seu nome e o seu e-mail.
Boa leitura!
Junho/2023
6-Perda da Visão
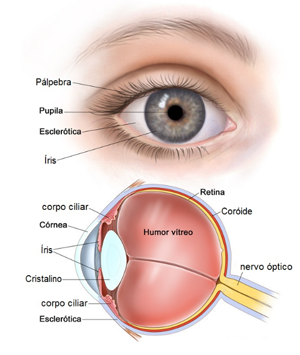
Figura 11 – Os cílios protegem os olhos contra materiais suspensos no ar, como a poeira. As pálpebras se movimentam (piscam) espalhando as lágrimas que umedecem a córnea e a esclerótica retirando substâncias prejudiciais ao olho
A visão é, provavelmente, dos nossos 5 sentidos o mais nobre. Nossos olhos são as janelas que nos permitem ver o mundo maravilhoso e colorido que nos rodeia e são também, os espelhos de nossos sentimentos e emoções. Como abordaremos o transplante de células-tronco para diferentes regiões oculares, segue abaixo um pequeno resumo.
A luz que chega aos nossos olhos percorre o seguinte caminho (veja Figura 11):
*Atravessa primeiramente a Conjuntiva, membrana transparente que recobre a parte anterior do olho e a parte interna das pálpebras (membrana que, se infeccionada causa a Conjuntivite);
*Depois passa ou pela Córnea, tecido transparente (feito de fibras paralelas de colágeno) que recobre a íris ou pela Esclerótica, tecido semirrígido (feito de fibras entrelaçadas de colágeno), opaco, que reflete a luz (dando a cor branca aos olhos) e que se estende até o nervo ótico. A córnea e a esclerótica estão ligadas pelo Limbo, tecido onde são geradas muitas células-tronco;
*Depois da córnea (a janela dos nossos olhos), a luz atravessa o Humor Aquoso líquido transparente, nutriente dessa região e que controla a pressão ocular;
*Em seguida vem a Íris, que é um músculo com muitos pigmentos (que dão a cor ao olho – marrom, mel, verde, cinza e azul) e que também controla o diâmetro de um orifício chamado Pupila. O diâmetro da pupila regula a intensidade de luz que seguirá adiante (quanto mais luz menor o diâmetro). Em ótica, a íris e a pupila corresponderiam ao diafragma e a abertura, respectivamente.
*Depois a luz passa pelo Cristalino que é uma lente transparente que se movimenta para focar objetos situados em diferentes distâncias. A Catarata é uma lesão que torna o cristalino menos transparente.
*Então, a luz atravessa o Humor Vítreo, substância transparente e gelatinosa que dá a forma esférica ao olho.
*Finalmente, a luz atinge a Retina que é uma camada de células fotossensíveis com formatos de bastonetes (120 milhões) e cones (6 milhões). A retina se apoia sobre um tecido chamado de Coróide, que contém uma rede de vasos sanguíneos fornecedora de oxigênio e nutrientes para a retina. O olho humano tem diâmetro de 2,2 cm, ou seja, uma área de aproximadamente 3,8 cm2. A retina recobre quase 70% dessa superfície. No centro dela se encontra uma pequena região (com raio de 0,5 cm) chamada Mácula e no interior dela, uma área menor ainda, alinhada com o eixo central da lente do cristalino, chamada de Fóvea. Elas são compostas somente por células cônicas. São responsáveis pela visão nítida e detalhada. A degeneração da mácula ocorre com o avanço da idade e é uma das doenças oculares que podem ser tratadas com células-tronco.
*As células receptoras transformam a luz em impulsos elétricos que são conduzidos pelo Nervo Ótico até o cérebro onde as imagens são formadas e interpretadas.
A-Retina
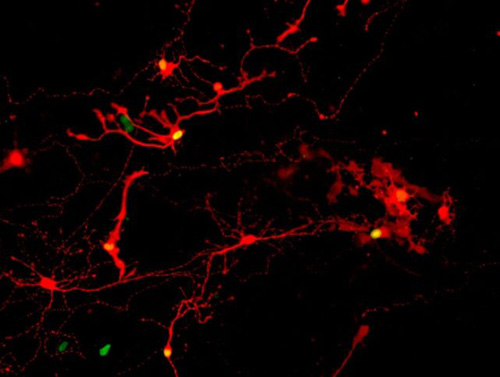
Figura 12 – Após a dissociação do organóide retinal, foi utilizado como marcador um vírus modificado da raiva. Em vermelho, o rastro deixado pelo marcador, demostrando a reconexão entre células fotorreceptoras e células ganglionares (Fonte: UW-Madison/Gamm Laboratory)
Nas doenças degenerativas da retina, as células fotorreceptoras começam a funcionar mal, morrem, levando à cegueira progressiva. Como vimos anteriormente, é natural lançar mão de células-tronco pluripotentes induzidas (ou não) para restaurar a retina repondo suas células fotossensíveis.
No início as culturas das células-tronco cresciam em duas dimensões (placas de Petri) mas, rapidamente os pesquisadores se convenceram de que, para os transplantes, era necessário fazer o cultivo em três dimensões. Essas culturas passaram a ser chamadas de organóides. Há várias técnicas para isso, mas basicamente todas elas utilizam hidrogel sintéticos ou biológicos.
Em 2014, pesquisadores da Universidade Johns Hopkins, Maryland, EUA, recriaram in vitro aspectos funcionais e estruturais da retina. Eles utilizaram células-tronco pluripotentes induzidas que foram obtidas a partir da pele humana. O organóide 3D assim construído, tinha a sequência correta das camadas correspondentes aos bastonetes e cones e eram fotossensíveis!
Para avançar para uma fase de testes clínicos era necessário provar que essa retina construída no laboratório, uma vez dissociada do organóide, manteria sua capacidade de formar novas conexões sinápticas. Isso foi demonstrado em um trabalho realizado por uma equipe da Universidade de Wisconsin e publicado em 2023 (Figura 12) na revista PNAS.
B-Mácula
A degeneração macular relacionada à idade é a lesão ocular mais comum para indivíduos com mais de 50 anos. Caracteriza-se pela perda progressiva de visão, com o surgimento de pontos escuros nos olhos; os objetos que estão bem à sua frente (pois, como vimos, a mácula fica bem no centro da retina) começam a perder a forma, o tamanho e a cor ou ficar embaçados; ao ler um texto, palavras podem desaparecer.
A degeneração da mácula neovascular (ou úmida) é a forma mais grave da doença. Nas pessoas com degeneração macular úmida, o Coróide se enche em demasia de vasos sanguíneos que acabam perfurando o epitélio pigmentar da retina, justamente onde ela é mais esgarçada – a mácula. O epitélio pigmentar da retina é a última camada da retina à qual estão ligados diretamente os fotorreceptores – cones e bastonetes.
A terapia tradicional dessa lesão consiste aplicar injeções intraoculares de medicamentos antiangiogênicos (que ajudam a secar os vasos sanguíneos) como Lucentis e Eylea. Esse tratamento não cura, não pode ser aplicado em casos de conjuntivite e flebite (inflamação nas veias das pernas) e é comum recidivas.
Em 2010, uma mulher japonesa de 77 anos foi diagnosticada com degeneração macular úmida. Passou 3 anos sendo medicada com antiangiogênicos, mas a doença era recorrente. Ao todo ela recebeu 13 injeções intraoculares que não conseguiram parar a degeneração!
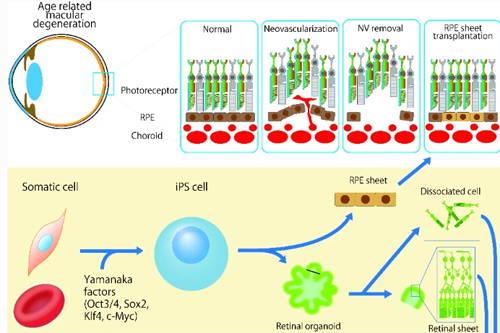
Figura 13 – Na parte de cima: olho normal, neovascularização com ruptura do epitélio pigmentar, remoção dessa região e transplante da cultura de células tronco induzidas a partir de células somáticas (na parte de baixo).
Em novembro de 2013, ela foi escolhida para fazer um tratamento clínico experimental. Nessa ocasião, sua acuidade visual era de 0,15 e 0,20 nos olhos esquerdo e direito, respectivamente. Esses valores foram obtidos usando-se anéis de Landolt. Estes anéis têm a forma aproximada de um C (o tamanho e a abertura do C são alterados e rotacionados pelo oftalmologista) e são bastante utilizados quando a pessoa não é alfabetizada. No Brasil é mais comum se utilizar a tabela de Snellen. Neste caso, a paciente teria 20/130 e 20/100 de acuidade visual.
A Medicina considera uma pessoa cega quando sua visão corrigida do seu melhor olho é menor ou igual a 20/200, ou seja, o que uma pessoa normal consegue enxergar a 50 m de distância, ela só consegue a 5m. Portanto, a idosa japonesa estava bem próxima da cegueira.
Depois de colhido material da paciente, utilizando-se protocolos bioquímicos para induzir células-tronco a se diferenciarem em células do epitélio pigmentar da retina, várias culturas e amostras foram testadas em camundongos para verificar elas tinham algum potencial cancerígeno. No mês de setembro de 2014, dez meses depois do início do tratamento clínico, foi realizado o primeiro transplante mundial desse tipo (Figura 13). O sucesso foi parcial, pois um ano depois da cirurgia, não houve aumento da acuidade visual, mas a progressão degenerativa foi estancada.
Agora em 2023, um grupo de pesquisa de Kobe (Japão) publicou uma revisão do método e estimou que esse primeiro transplante, além de demorado, teria custado cerca de um milhão de dólares. Eles propõem a utilização de técnicas de HLA (Human Leukocyte Antigens) para diminuir o tempo e o dinheiro necessários para o transplante.
C-Córnea
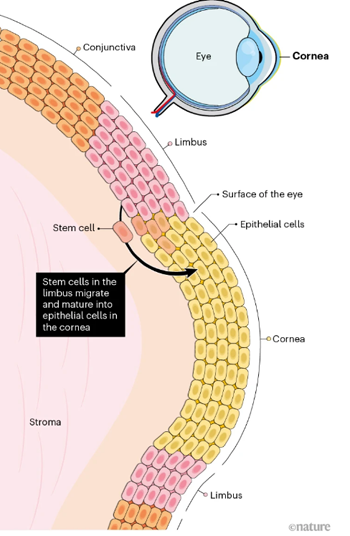
Figura 14 – O limbo é uma região rica em células-tronco. Elas se diferenciam e migram para formarem as células epiteliais da córnea (Fonte: Nature)
Como dissemos na Introdução, o primeiro transplante de córnea foi realizado em 1905 pelo médico austríaco E. Zirm. O receptor foi um trabalhador rural de 45 anos que, ao limpar um galinheiro com cal, teve seus dois olhos queimados. O doador da córnea foi um menino de 11 anos, cego por perfuração das duas escleróticas. Suas córneas foram removidas e enxertadas no agricultor. No olho direito a cirurgia falhou, mas o esquerdo atingiu, depois de 6 meses, acuidade visual 6/36 (ou seja, ele conseguia ver a 6 metros de distância o que uma visão normal consegue a 36 metros).
Muito embora o primeiro transplante de córnea tenha sido feito com um doador vivo, toda pessoa com córneas sadias e que tenha falecido há menos de 6 horas (ou 24 horas, mas congelada) pode ser um doador. Como a córnea não contém vasos sanguíneos, não importa o tipo sanguíneo do doador e do receptor.
Com um índice de sucesso entre 80 a 90 % dos transplantes, o número de cirurgias da córnea realizadas por ano é de cerca de 185 mil no mundo e 13 mil no Brasil. As técnicas desses transplantes evoluíram muito ao longo do tempo e se tornaram extremamente precisas com a utilização de lasers.
Um transplante de córnea pode não ter resultado positivo se o limbo (a região entre conjuntiva e a córnea) não produzir ou for deficiente na reposição das células epiteliais da córnea (veja figura 14).
Quando essa deficiência ocorre somente em um dos olhos, parte das células-tronco são cirurgicamente removidas, crescidas em laboratório e colocadas no limbo danificado. Mas, quando o problema está presente em ambos os olhos, entram em cena as células-tronco pluripotentes induzidas.
O primeiro transplante desse tipo foi feito em uma mulher japonesa pelo cirurgião Kohji Nishida, da Universidade de Osaka, em 2019. Não houve rejeição.
Um programa mais ambicioso está em andamento na Universidade de New Castle (Reino Unido). Utilizando uma impressora 3D com uma tinta composta por células-tronco pluripotentes, colágeno e um extrato de alga, os pesquisadores Swioklo e Connon pretendem construir uma córnea completa!
7-Perspectivas
Quase todas as doenças danificam, de alguma forma, os tecidos do nosso corpo quer sejam elas oriundas de infecções, doenças crônicas ou degenerativas. A reparação de tecidos danificados, quando não eficiente, acaba redundando na formação de fibroses. A fibrose pode afetar qualquer órgão e está particularmente presente em processos inflamatórios crônicos. Estima-se que 45% de todas as mortes podem ser mapeadas, em última instância, a falhas regenerativas associadas à fibrose e inflamações.
Como vimos, a medicina regenerativa muito se desenvolveu nesta última década, mas muito ainda está para ser feito. Segundo artigo recente publicado na revista Nature, os maiores obstáculos aos avanços da medicina regenerativa (veja Figura 15) são: inadequação das células progenitoras (escassez de células-tronco, comprometimento funcional e status de diferenciação), inflamação e fibrose. Por outro lado, as terapias emergentes mais promissoras para a medicina regenerativa são: células-tronco humanas pluripotentes (tratadas nesta série de 3 artigos que ora encerramos), terapias anti-inflamatórias e anti-fibróticas. Neste último caso, está incluída a terapia celular CAR-T que levou, recentemente, à remissão de um paciente SUS com linfoma.
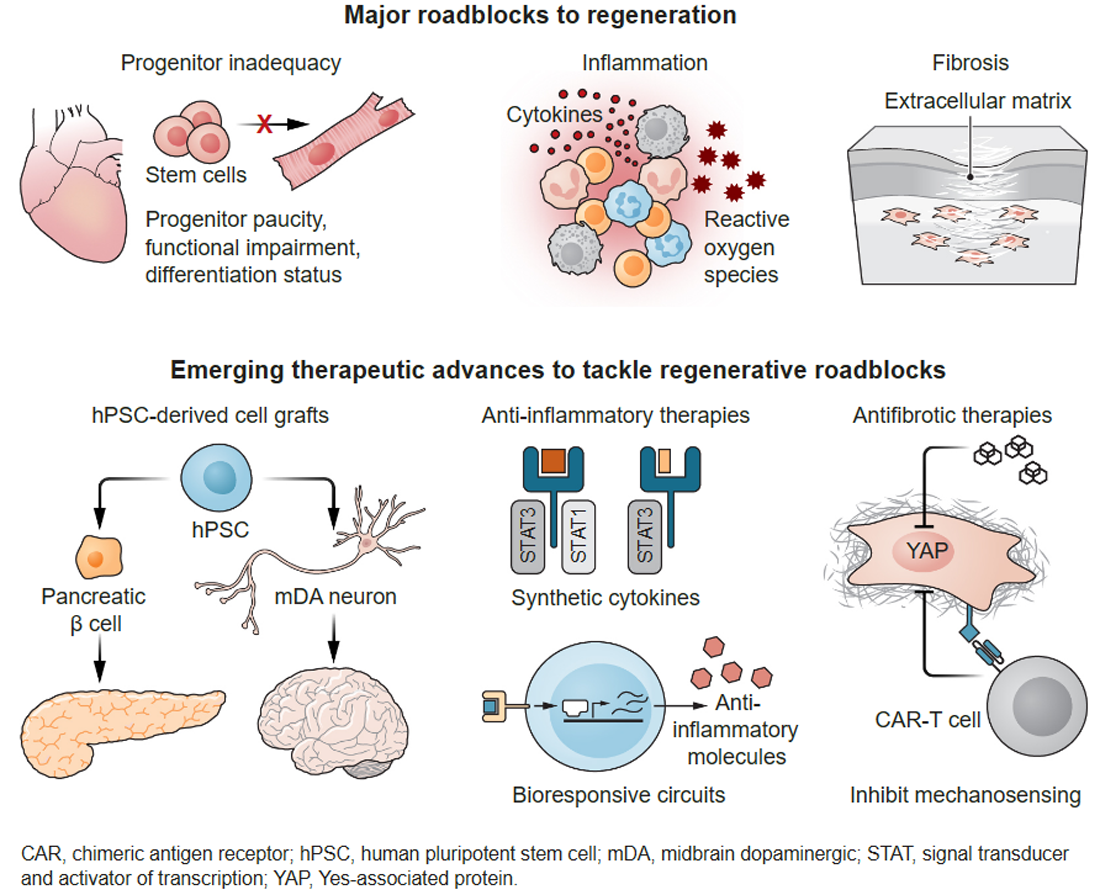
Figura 15 – Obstáculos à medicina regenerativa e terapias emergentes (Fonte: K. Holoski/Science)
*Físico, Professor Sênior do IFSC – USP
e-mail: onody@ifsc.usp.br
Para acessar todo o conteúdo do site “Notícias de Ciência e Tecnologia” dirija a câmera do celular para o QR Code abaixo:

Se você gostou, compartilhe o artigo nas redes sociais

(Agradecimento: ao Sr. Rui Sintra da Assessoria de Comunicação)
Assessoria de Comunicação – IFSC/USP




