
Figura-1: A membrana de celulose (superhidrofílica) produzida pela bactéria Gluconacetobacter hansenii é ótima para separar o óleo da água (Crédito: Zahra Ashrafi)
Por: Prof. Roberto N. Onody *
Deixe um prato sem lavar, por um certo tempo, e você notará a formação de um produto viscoso – um biofilme feito por bactérias. Tipos diferentes de bactérias produzem biofilmes diferentes.
A Gluconacetobacter hansenii é uma bactéria que oxida o açúcar ou o etanol e produz ácido acético. Essas bactérias são verdadeiras fabricas de celulose (C6H10O5)n, o mesmo material encontrado nos tecidos vegetais e que dá firmeza às plantas, só que muito mais puros. A rede de microfibras de celulose (veja Figura 1), fabricada pela Gluconacetobacter hansenii, adora água e forma uma membrana superhidrofílica. Essa membrana é o lar dessas bactérias, elas vivem ali.
Pesquisadores da Universidade do Estado da Carolina do Norte publicaram recentemente, na revista Langmuir 1, um estudo mostrando a extraordinária capacidade dessa membrana de separar e filtrar o óleo da água. Depois de removerem as bactérias e os resíduos de não celulose, o que sobra é uma membrana de celulose muito pura e robusta (Figura 2). Para que essa membrana se torne um excelente filtro é necessário que ela esteja embebida em água. Em outras palavras, a água deve molhar a membrana. Recapitulemos, brevemente, a teoria de quando um líquido molha (ou não) uma superfície.
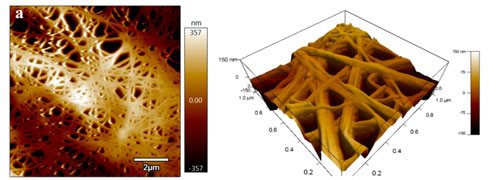
Figura-2: À esquerda, imagem da membrana (seca) feita por microscópio de força atômica, mostrando a variação de sua espessura (em nanômetros) e o entrelaçamento das nanofibras de celulose. À direita, imagem em 3D, apresentando a microestrutura dos poros (Crédito: Z. Ashrafi et al. 1)
O estudo de molhamento de uma superfície, envolve as 3 fases – líquida (L), sólida (S) e gasosa (G). As moléculas que se encontram na fronteira, entre uma fase A e B, interagem entre si com um conjunto de forças bem diferentes daquelas envolvendo as moléculas que se encontram no interior da fase A ou da fase B (as forças de coesão). Essas forças são chamadas de tensões superficiais: γSL, γSG e γLG. Para uma superfície sólida rígida, lisa, plana e quimicamente homogênea (veja Figura 3), T. Young deduziu, em 1805, a relação de Young γSG = γSL + γLG cos(θC) que se obtém da 2ª. Lei de Newton para o equilíbrio das componentes horizontais das forças. Na vertical, o equilíbrio se faz pelas forças de adesão e θC é o ângulo de contacto. Se a superfície não é quimicamente homogênea, haverá uma distribuição (histerese) de ângulos de contacto, entre um valor máximo e mínimo.
Se o líquido for água (óleo) e molhar o substrato então, a superfície é chamada hidrofílica (oleofílica) e hidrofóbica (oleofóbica), caso contrário. Se θC > 150o, diz-se que ela é superhidrofóbica (superoleofóbica). É o que acontece, por exemplo, com a água nas pétalas da flor de Lotus ou num tecido impermeabilizado.
Superfícies reais não são lisas, mas sim, rugosas. Há dois modelos que descrevem o molhamento de superfícies rugosas.
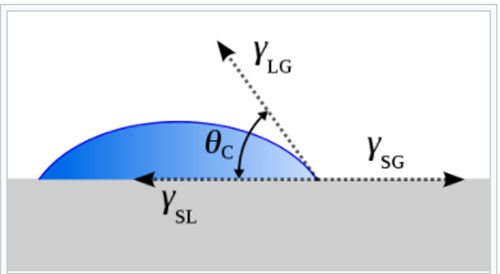
Figura-3: As tensões superficiais entre as fases sólida, líquida e gasosa e o ângulo de contacto θC (Crédito: ref. 2)
No modelo de Wenzel (Figura 4), o líquido penetra a superfície rugosa no ponto de contacto. Devido à rugosidade, a área da interface líquido-sólido, aumenta por um fator r. O líquido molha toda a área da interface. O novo ângulo de contacto θ* passa a ser descrito pela equação de Wenzel cos(θ*) = r cos(θC)
No modelo de Cassie (Figura 5), o líquido molha somente uma fração f da interface. Há bolsões de ar armadilhados. A equação de Cassie se escreve cos(θ*) = r f cos(θC) + f – 1
Se f = 1, recuperamos a equação de Wenzel. Voltemos agora, ao artigo de Z. Ashrafi et al. 1.
A separação do óleo da água é de suma importância no socorro ambiental, seja pelo derramamento de óleo ou tratamento do esgoto industrial. Há algumas décadas, a pesquisa cientifica se concentrou em membranas com superfícies superhidrofóbica-superoleofílica (chamadas de removedoras de óleo), muitas delas, contendo perigosos componentes a base de fluoretos. Mas, há dois problemas com essas membranas.
O primeiro é que, à medida que o óleo se acumula sobre a membrana, ela perde seu caráter superoleofílico, diminuindo o fluxo de separação. O óleo tem que ser removido e reciclado, o que diminui o tempo de vida do material. O segundo é que a água é mais densa do que o óleo e uma separação, guiada pela gravidade, não é possível.

Figura-4: O modelo de Wenzel é apropriado para sistemas em que o líquido e a superfície rugosa têm fortes forças de adesão (Crédito: ref. 2)
Pensou-se, então, em fazer uma inversão dessas propriedades e se utilizar membranas com superfícies, simultaneamente, superhidrofílica e superoleofóbica (também chamadas de removedoras de água). Porém, se uma superfície tem energia suficientemente baixa para repelir o óleo, ela também repelirá a água, pois esta tem fortes forças de coesão, devido à presença de uma rede de pontes de hidrogênio. A tensão superficial da água é maior do que a dos óleos. Portanto, encontrar superfícies superoleofóbicas é um desafio.
A solução veio através de inspiração biológica. A escama dos peixes é superoleofóbica, com ângulo de contacto (do óleo com a escama) em torno de 156o. A explicação está no fato de as escamas possuírem micro e nano estruturas nas escamas com camadas de hidrogel cheias de água3 (o muco). Como a celulose produzida pela Gluconacetobacter hansenii tem estrutura semelhante, se infiltrarmos essa membrana com água, antes de iniciarmos a filtragem, a superfície atrairá moléculas de água e repelirá gotas de óleo (Figura 6). Se fizermos passar pela membrana de celulose embebida em água, uma corrente de mistura água e óleo (com pressão externa ou usando a própria ação da gravidade) o óleo ficará retido.

Figura-5: O modelo de Cassie é mais apropriado para sistemas em que o líquido e a superfície rugosa têm fracas forças de adesão (Crédito: ref. 2)
Os autores da pesquisa1 estudaram membranas biosintéticas de celulose. As nanofibras emaranhadas possuíam um diâmetro médio de 35 nanômetros, formando um substrato, em que a rugosidade da superfície tinha um raio quadrático médio de cerca de 57 nanômetros. Essas membranas eram então aquecidas num forno para secar e, depois de resfriadas, eram pesadas, mergulhadas em água e novamente pesadas. A capacidade média de absorção de água foi de 98,3 %, para membranas com uma espessura média de 1 mm. O valor médio estimado do ângulo de contacto do óleo com a membrana foi de 174,5o, revelando ser ela superoleofóbica. O óleo utilizado foi o n-dodecano C12 H26, cuja tensão superficial, à temperatura ambiente, vale 25 dinas/cm (contra 72 dinas/cm da água).
Finalmente, vamos analisar os resultados dos experimentos. Uma mistura de água e óleo atravessa as biomembranas (com ou sem pressão externa) e mede-se a eficiência da filtragem ε, definida por ε (%) = 100 (1 – Cf /Ci), onde, Cf é a concentração de óleo (em mg) final, depois da filtragem e Ci é a concentração de óleo (em mg) inicial, antes da filtragem. O resultado foi muito bom. Eles obtiveram ε = 99,9% à pressão de 2,3 atm e ε=99,0% à pressão de 1 atm.
Vejamos as razões para tão bom desempenho. A celulose que compõe a membrana é naturalmente hidrofílica, pois contém muitos grupos de hidroxila, que permitem a formação de pontes de hidrogênio com as moléculas da água. A água embebida na membrana, tem forte força de coesão com as moléculas da água contida na mistura óleo-água. Forma-se, sobre a membrana, uma película de água que repele o óleo, mas deixa fluir a água. Segundo os pesquisadores, esse sistema pode ser bem descrito pelo modelo de Cassie.
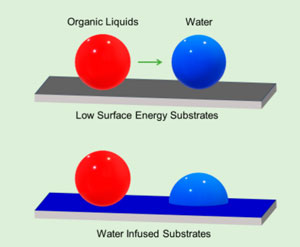
Figura-6 No alto, um substrato com baixa energia superficial repele tanto as gotas de óleo quanto as de água. Embaixo, o mesmo substrato embebido em água permite a passagem de água, mas repele o óleo (Crédito: Z. Ashrafi et al. 1)
No Brasil, a cepa bacteriana Gluconacetobacter hansenii também tem sido bastante estudada nos seus mais diferentes aspectos: produção e caracterização da celulose 4, tratamento de lesões da pele 5, aplicações em cosméticos 6 e sequenciamento do genoma 7.
*Físico, Professor Sênior do IFSC – USP
(Agradecimento: ao Sr. Rui Sintra da Assessoria de Comunicação)
Referências:
1 Z. Ashrafi, Z. Hu, L. Lucia e W. Krause, Langmuir 2021, 37, 2552−2562
https://doi.org/10.1021/acs.langmuir.0c02717
2 https://en.wikipedia.org/wiki/Wetting
3 Z. Ashrafi, Z. Hu, L. Lucia e W. Krause, ACS Appl. Mater. Interfaces 2019, 11, 21275−21293
4 Revista Matéria, V. 25, no. 4, ISSN 1517-7076 artigos e12844, 2020
5 https://periodicos.ufjf.br/index.php/enfermagem/article/view/3809
6 J. D.P. de Amorim et al., DOI:10.34117/bjdv5n10-099
7https://por.kyhistotechs.com/genome-sequence-plasmid-transformation-model-high-yield-bacterial-cellulose-producer-gluconacetobacter-78520097
Assessoria de Comunicação – IFSC/USP




